近日,华东理工大学上海多级结构纳米材料工程技术研究中心李春忠教授和顾金楼教授课题组,报道了铈基金属有机骨架(Ce-MOF)具有独特的类腺苷三磷酸双磷酶活性,能够高效催化高能磷酸键的水解,实现并干预三磷酸腺苷(ATP)和二磷酸腺苷(ADP)分子的脱磷酸化过程。该工作以“Intrinsic Apyrase-Like Activity of Cerium-Based Metal-Organic Frameworks: Dephosphorylation of Adenosine Tri- and Diphosphate”为题,发表于Angew. Chem. Int. Ed. 期刊,得到审稿人和编辑的高度认可,认为对ATP/ADP参与的生命活动过程具有重要的意义,并被推荐为VIP论文,被国际权威学术新闻媒体ChemistryViews 作为亮点评述。
ATP和ADP作为重要的生物信号分子,参与许多生理过程,如血液凝结、炎症和免疫反应、能量代谢等。腺苷三磷酸双磷酶作为一类重要的细胞外酶,通过高效催化ATP和ADP的高能磷酸键水解,调节生理过程和推动生命活动。因此,发展能够模拟腺苷三磷酸双磷酶的仿生材料,实现ATP和ADP分子的脱磷酸化过程,有着重要的意义。
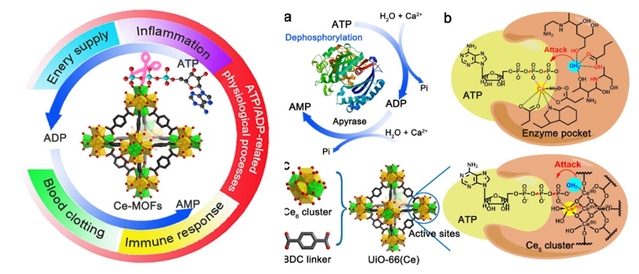
近年来,金属有机骨架(MOFs)作为一类快速发展的多孔晶体材料,它们的有序多孔结构提供了丰富和高活性的金属位点,使MOFs作为仿生催化材料具有独特的吸引力。研究人员发现:与天然腺苷三磷酸双磷酶相比,仿生的Ce-MOF具有二价阳离子独立性,不依赖于钙离子作为辅因子以结合和极化ATP 或ADP的末端磷酸基团,同时具有宽泛的工作条件和出色的稳定性。能够在生理条件下,选择性催化水解ATP和ADP的末端磷酸酯键,而对AMP和其他非核苷磷酸酯中的磷酸单酯键不具有显著的水解活性。在脱磷酸化机制中,Ce(IV)-OH起到了关键性作用,Ce(IV)能够有效地结合和极化ATP的高能磷酸键,使其能够受到表面羟基或水分子的亲核进攻而水解;而少量Ce(III)可能作为协同位点,促进水分子的亲核进攻,提高水解效率。
细胞外ADP作为重要的信号分子,能够诱导血小板聚集。作者通过制备柔性的Ce-MOF薄膜,发现膜材料对ADP诱导的血小板聚集有着显着的抑制作用。考虑到ATP和ADP的脱磷酸化过程在生命活动中具有重要地位,该工作为设计和发展模拟腺苷三磷酸双磷酶的仿生材料,干预和调节ATP和 ADP相关的生理过程,提供了一种新的策略。
该论文主要由博士后杨健在李春忠教授和顾金楼教授的指导下完成,该研究得到了国家自然科学基金和上海市自然科学基金的支持。
原文链接:
https://onlinelibrary.wiley.com/doi/10.1002/anie.202008259
ChemistryViews链接:
https://www.chemistryviews.org/details/ezine/11269030/MOFs_with_Enzyme-Like_Activity.html